O Que É Solução Solvente E Soluto Dê Exemplos – O Que É Solução Solvente E Soluto? Dê Exemplos. No mundo da química, as soluções desempenham um papel fundamental em inúmeras aplicações. Uma solução é uma mistura homogênea de duas ou mais substâncias, onde uma substância (soluto) é dissolvida em outra (solvente).
Compreender a natureza das soluções solventes e solutos é essencial para entender vários processos químicos e suas aplicações práticas.
Neste artigo, exploraremos o conceito de soluções solventes e solutos, examinaremos seus diferentes tipos e propriedades e discutiremos suas aplicações em vários campos. Além disso, forneceremos exemplos específicos para ilustrar esses conceitos e responderemos a perguntas frequentes sobre o assunto.
Definição de Solução Solvente e Soluto
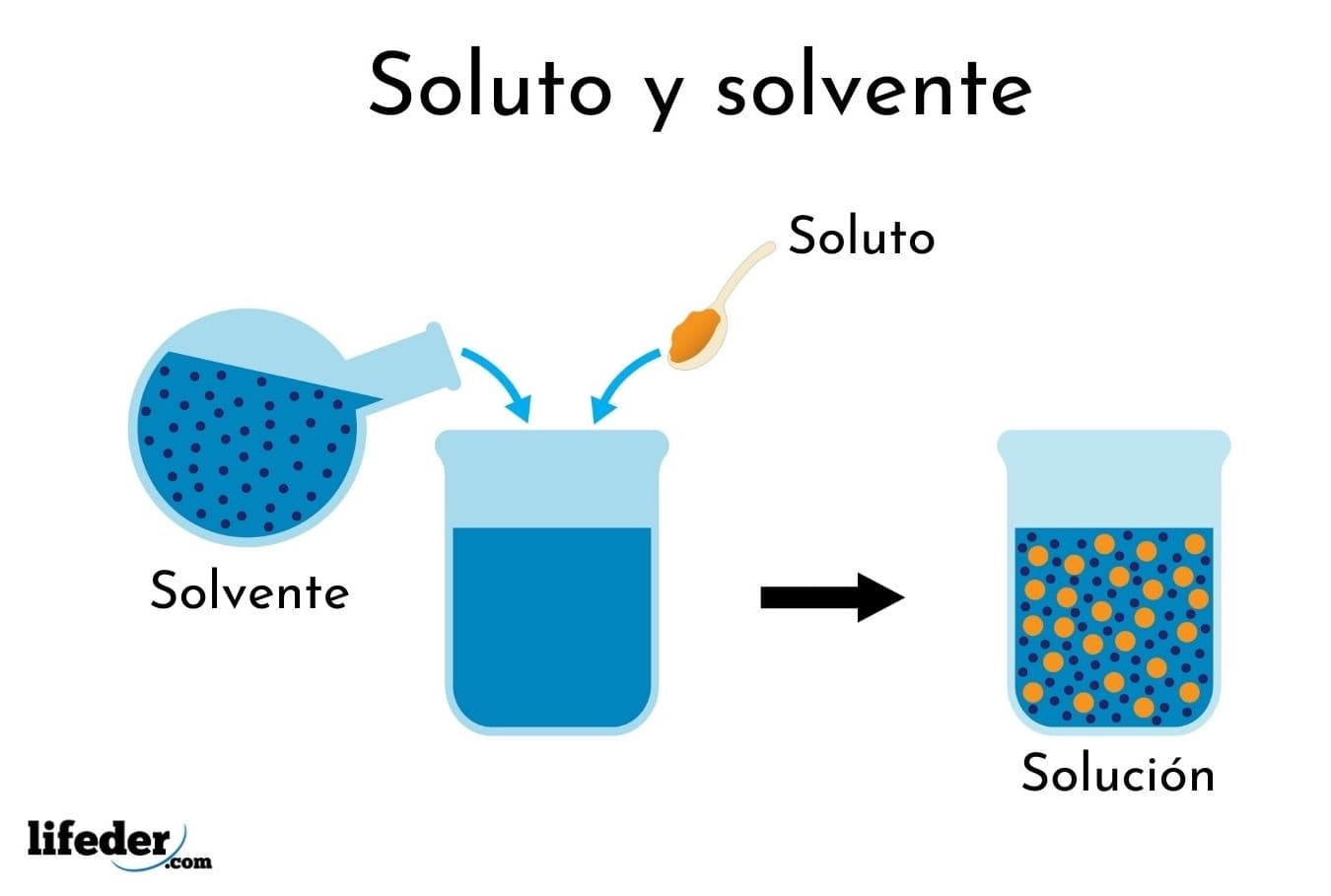
Uma solução é uma mistura homogênea de duas ou mais substâncias. Os componentes de uma solução são chamados de solvente e soluto.
Solvente
O solvente é a substância presente em maior quantidade na solução. Ele dissolve o soluto, formando uma mistura homogênea.
Soluto
O soluto é a substância presente em menor quantidade na solução. Ele é dissolvido pelo solvente, formando uma mistura homogênea.
Exemplos de Soluções Solventes e Solutos
Alguns exemplos de soluções solventes e solutos são:
- Água (solvente) + Sal (soluto)
- Álcool (solvente) + Iodo (soluto)
- Benzeno (solvente) + Tolueno (soluto)
Tipos de Soluções Solventes
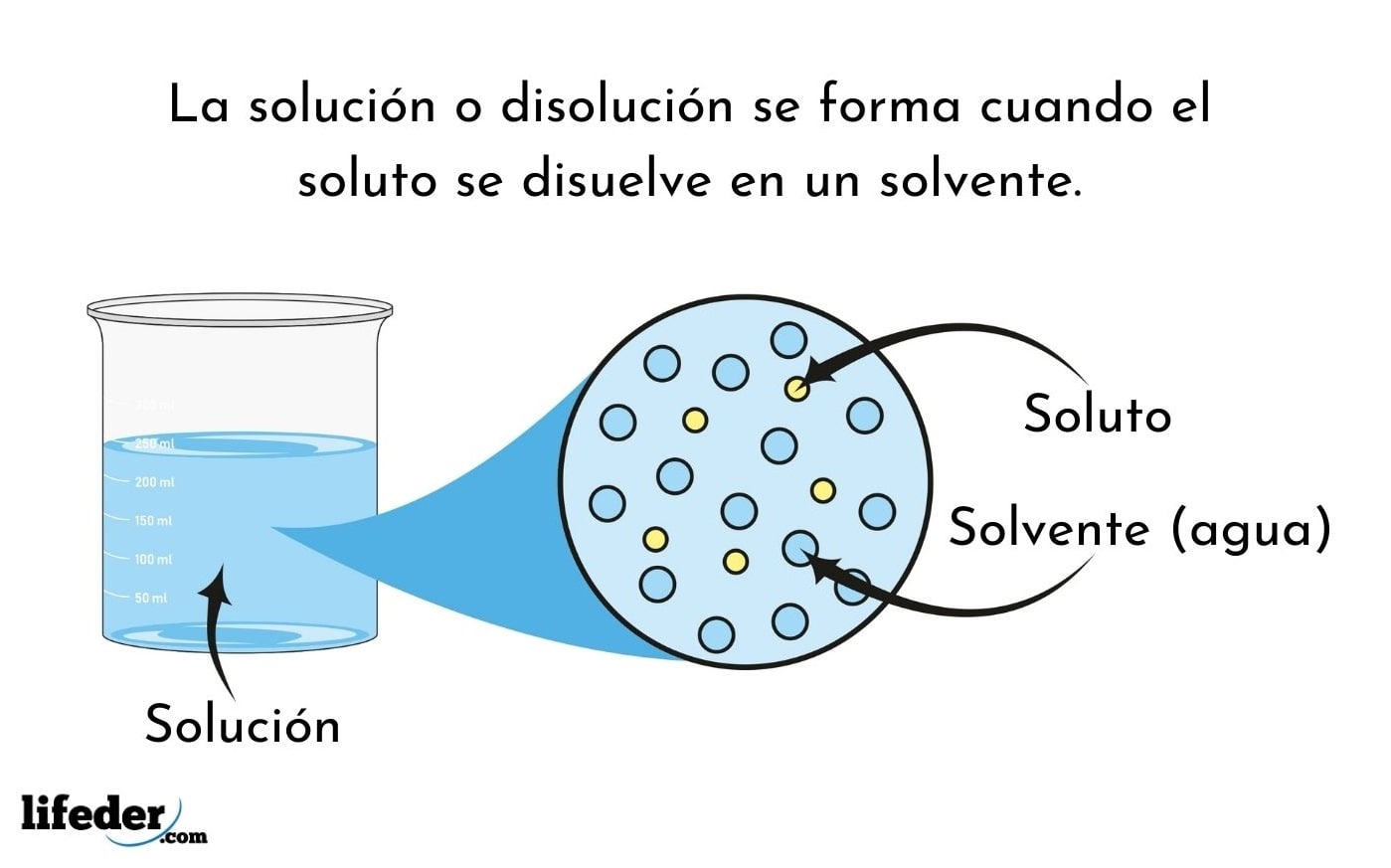
As soluções solventes podem ser classificadas em diferentes tipos com base em suas propriedades e características. Os três principais tipos de soluções solventes são aquosas, orgânicas e não aquosas.
Soluções Aquosas
As soluções aquosas são aquelas em que o solvente é a água. A água é um solvente polar, o que significa que possui uma distribuição desigual de cargas elétricas. Isso permite que ela dissolva facilmente substâncias polares, como sais, açúcares e proteínas.
- Propriedades: Polares, boa capacidade de dissolução para substâncias polares.
- Exemplos: Água salgada, soluções de açúcar, bebidas esportivas.
Soluções Orgânicas
As soluções orgânicas são aquelas em que o solvente é um composto orgânico, como álcool, éter ou benzeno. Os solventes orgânicos são geralmente apolares, o que significa que não possuem uma distribuição desigual de cargas elétricas. Isso permite que eles dissolvam facilmente substâncias apolares, como óleos, gorduras e ceras.
- Propriedades: Apolares, boa capacidade de dissolução para substâncias apolares.
- Exemplos: Tinta, removedor de esmaltes, gasolina.
Soluções Não Aquosas
As soluções não aquosas são aquelas em que o solvente não é nem água nem um composto orgânico. Elas podem ser compostas por solventes inorgânicos, como amônia ou dióxido de enxofre, ou por misturas de solventes. As soluções não aquosas são usadas em uma variedade de aplicações, como limpeza, fabricação de medicamentos e síntese química.
- Propriedades: Podem ser polares ou apolares, dependendo do solvente usado.
- Exemplos: Amônia líquida, solução de iodo em álcool, hexano.
Propriedades das Soluções Solventes
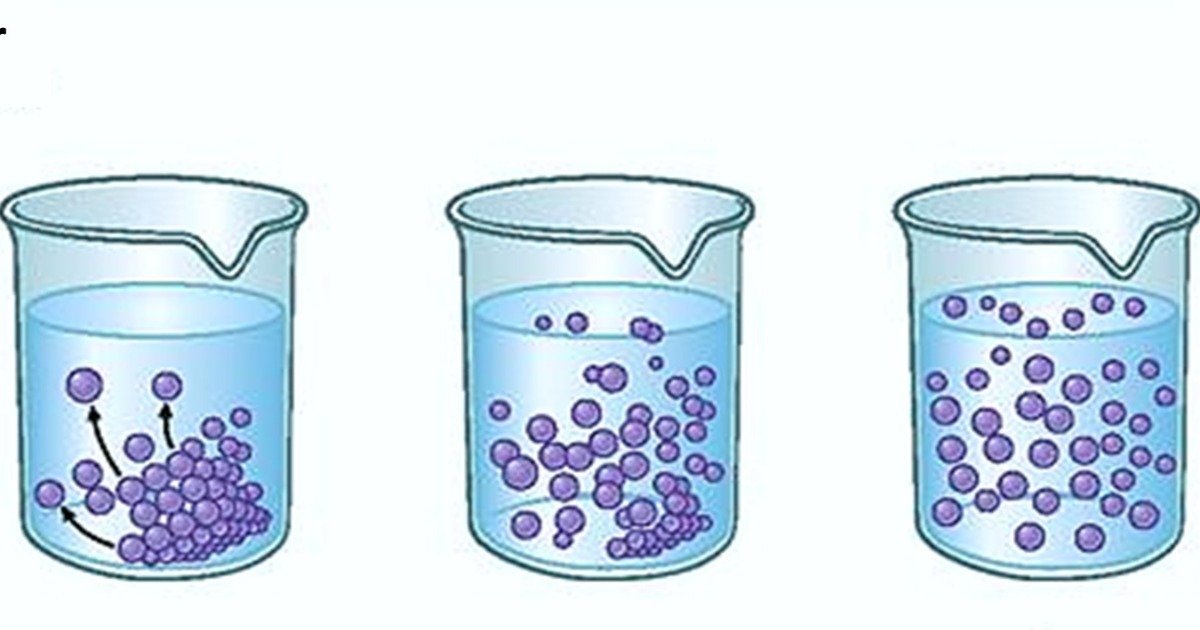
As soluções solventes exibem propriedades distintas que influenciam o comportamento da solução. Essas propriedades incluem concentração, solubilidade e polaridade.
A concentração mede a quantidade de soluto dissolvido em uma determinada quantidade de solvente. Ela pode ser expressa em várias unidades, como molaridade (mol/L) ou porcentagem em massa.
A solubilidade refere-se à quantidade máxima de soluto que pode ser dissolvido em um determinado solvente em condições específicas. Ela depende da natureza do soluto e do solvente, bem como da temperatura e pressão.
A polaridade é uma medida da separação de carga dentro de uma molécula. Solventes polares têm uma distribuição desigual de carga, enquanto solventes apolares não. A polaridade do solvente afeta sua capacidade de dissolver solutos polares ou apolares.
Métodos de Medição e Controle, O Que É Solução Solvente E Soluto Dê Exemplos
Existem vários métodos para medir e controlar as propriedades das soluções solventes.
- A concentração pode ser medida usando titulação, espectrofotometria ou cromatografia.
- A solubilidade pode ser determinada por meio de experimentos de saturação ou métodos espectrofotométricos.
- A polaridade pode ser avaliada usando o parâmetro de constante dielétrica ou o índice de refração.
Aplicações das Soluções Solventes

As soluções solventes encontram aplicações diversas em vários campos, incluindo química, indústria e medicina. Essas aplicações são possíveis devido às propriedades únicas das soluções solventes, como sua capacidade de dissolver e misturar substâncias.
Química
-
Soluções solventes são usadas como reagentes em reações químicas. Elas podem dissolver reagentes sólidos ou líquidos, facilitando sua mistura e aumentando a taxa de reação.
-
As soluções solventes são usadas para extrair compostos de misturas. Um solvente adequado pode dissolver o composto desejado, enquanto deixa outros componentes intactos.
-
As soluções solventes são usadas para purificar substâncias. Um solvente pode dissolver as impurezas de uma substância, que podem ser posteriormente separadas por filtração ou destilação.
Soluções Solventes em Reações Químicas: O Que É Solução Solvente E Soluto Dê Exemplos

As soluções solventes desempenham um papel crucial em reações químicas, influenciando sua velocidade e equilíbrio. As propriedades do solvente, como polaridade, constante dielétrica e ponto de ebulição, podem afetar significativamente o comportamento dos reagentes e produtos.
Influência das Propriedades do Solvente
- Polaridade:Solventes polares, como água, dissolvem solutos polares e iônicos, enquanto solventes apolares, como hexano, dissolvem solutos apolares.
- Constante dielétrica:Uma alta constante dielétrica indica a capacidade do solvente de reduzir as forças eletrostáticas entre íons, aumentando a solubilidade de compostos iônicos.
- Ponto de ebulição:Solventes com pontos de ebulição mais baixos são mais voláteis e podem ser facilmente removidos após a reação.
Papel do Solvente em Reações Específicas
- Reações de precipitação:Solventes polares, como água, promovem a precipitação de compostos iônicos devido à sua capacidade de solvatar íons.
- Reações de neutralização:Solventes polares, como água, fornecem um meio para a dissociação de ácidos e bases, facilitando a reação de neutralização.
- Reações orgânicas:Solventes apolares, como hexano, são usados em reações orgânicas para dissolver reagentes e produtos apolares.
Em resumo, as soluções solventes e solutos são componentes cruciais em muitos processos químicos e aplicações práticas. Compreender sua natureza, tipos e propriedades é essencial para manipular e utilizar soluções com eficácia. Ao explorar o mundo das soluções, os cientistas e pesquisadores podem desbloquear novas possibilidades e avanços em vários campos.
Quick FAQs
O que é uma solução?
Uma solução é uma mistura homogênea de duas ou mais substâncias, onde uma substância (soluto) é dissolvida em outra (solvente).
Qual é a diferença entre solvente e soluto?
O solvente é a substância presente em maior quantidade na solução e dissolve o soluto. O soluto é a substância presente em menor quantidade e é dissolvido pelo solvente.
Quais são os diferentes tipos de soluções solventes?
Existem vários tipos de soluções solventes, incluindo aquosas (solvente: água), orgânicas (solvente: composto orgânico) e não aquosas (solvente: líquido não aquoso).


